Branchen
März 2023
Normen sollen über Spezifikationen, Verfahren und Richtlinien gewährleisten, dass ein Produkt sicher, konsistent und zuverlässig ist. Für ein medizinisches elektrisches Gerät sind elektrische Sicherheitsnormen von grösster Bedeutung. Doch obwohl sie in erster Linie als Orientierungshilfe dienen sollen, werden sie oft als Herausforderung empfunden. Als Entwicklungspartner verfügt Helbling über umfassende Erfahrung in der Arbeit mit der IEC 60601 Normenfamilie, welche die grundlegende Sicherheit (Basic Safety) und die wesentlichen Leistungsmerkmale (Essential Performance) von medizinischen elektrischen Geräten abdeckt. Hier geben Helbling-Fachleute fünf Tipps, wie die Anforderungen erfolgreich erfüllt werden können, ohne dass der Aufwand zu gross wird.
Tipp 1: Konformität ist nicht erreichbar, wenn die Norm erst am Ende der Entwicklung berücksichtigt wird.
Es ist häufig zu beobachten, dass Unternehmen die Einhaltung der Normen als Teil des Verifizierungsprozesses einplanen und diese zuvor keine Rolle spielen. Das ist ein grundlegender Fehler: Die Erfüllung der IEC 60601-Norm ist eine komplexe und vielschichtige Aufgabe. Es handelt sich nicht nur um eine Liste von Tests, die dem Verifizierungsplan hinzugefügt werden. Die IEC 60601-Normenfamilie bietet eine Anleitung für die ordnungsgemässe Konstruktion eines medizinischen elektrischen Geräts. Wird dies nicht früh genug berücksichtigt, könnten eine ganze Reihe von Anforderungen übersehen werden, was im Nachhinein schwer zu korrigieren ist.
Je früher die Normen bei der Entwicklung berücksichtigt werden, desto grösser sind die Chancen, dass die Entwicklungsschleifen reduziert werden und sich die Zeit bis zur Markteinführung verkürzt.
Tipp 2: Gebrauchstauglichkeit, Dokumentation und Risikomanagement sind entscheidend.
Neben den Tests gehört zur Einhaltung der Normen auch die Überprüfung der wichtigsten Design-Dokumente, wobei Gebrauchstauglichkeit und Risikomanagement besonders wichtig sind.
Eine frühzeitige Risikoanalyse hilft bei der Definition der Essential Performance des Produkts. Dabei handelt es sich um andere klinische Funktionen als die der Basic Safety, deren Verlust oder Beeinträchtigung zu einem inakzeptablen Risiko führt.
Zu Beginn der Entwicklung müssen die Produkt-Vision und die wichtigsten klinischen Ansprüche definiert werden. Es muss zum Beispiel entschieden werden, wer das Produkt benutzen wird (etwa Patienten oder Ärzte), wie es aussehen wird oder wo es benutzt werden soll.
Eine wichtige Aufgabe besteht also darin, diejenigen Personen zu definieren und zu gruppieren, die das Produkt berühren oder verwenden dürfen. Wenn ein Medizinprodukt nur von gut ausgebildeten Fachleuten in einer kontrollierten Umgebung verwendet wird, werden manche Tests obsolet, oder die Risiken können durch Warnhinweise in der Gebrauchsanweisung minimiert werden. Wird das Produkt von einem Patienten allein zu Hause verwendet, sind die Risikominderungen in der Regel konservativer: Es muss auch die Altersgruppe des Anwenders, sein Allgemeinwissen und der Grad seiner Beeinträchtigung berücksichtigt werden. Auf diesen Punkt wird auch in einer ergänzenden Norm für sogenanntes Home Healthcare equipment eingegangen.
Darüber hinaus muss die Umgebung, in der das Gerät verwendet wird, in der Risikomanagement-Akte definiert werden. Daraufhin werden Grenzwerte festgelegt, gegen die das Gerät getestet wird. Unterschieden wird etwa zwischen einer Umgebung in einer professionellen Gesundheitseinrichtung und einer häuslichen Gesundheitsumgebung. Beispielsweise unterscheiden sich die Grenzwerte für elektromagnetische Emissionen und Interferenzen für einen Krankenhausmonitor in einer kontrollierten Umgebung von den Grenzwerten, die für ein medizinisches Gerät für den Heimgebrauch zu berücksichtigen sind.
Tipp 3: Die Norm sollte richtig verstanden werden.
Es sollte stets die letztgültige Version der Norm verwendet werden. Die Änderungen der Norm können sich manchmal auf wichtige Aspekte des Designs auswirken. So wurden etwa neue digitale Funktechnologien in früheren Versionen nicht berücksichtigt. Wichtig sind zudem die für medizinische elektrische Geräte geltenden Nebennormen, die die allgemeine Norm ausser Kraft setzen können.
Normen sind zudem nicht frei von Fehlinterpretationen. Diese Art von Fehlern kann dazu führen, dass wichtige Aspekte übersehen werden oder dass ein sogenanntes Overdesigning stattfindet, um Abschnitte zu erfüllen, die gar nicht gelten. Es gab Fälle, in denen das Gehäuse eines medizinischen Geräts nach den Anforderungen eines Brandschutzgehäuses konstruiert wurde, obwohl das für diese geringe Leistung nicht nötig war.
Die Normen bieten aber auch einen gewissen Spielraum bei der Erfüllung der Anforderungen. Beispielsweise ist es in Bezug auf den Schutz vor elektromagnetischen Störungen manchmal möglich, entweder eine zusätzliche Abschirmung am Gerät anzubringen, oder einfach in der Gebrauchsanweisung zu vermerken, dass das Gerät von Störquellen entfernt werden soll. Dafür ist es erforderlich, eine Risikoanalyse durchzuführen, die Abhilfemassnahmen zu dokumentieren und den Patienten zu informieren.
Im Zweifel lohnt es sich, einen Experten zu befragen – ein Re-Design ist teurer.
Schliesslich wird empfohlen, einen Blick in die Anhänge der Norm zu werfen. Sie enthalten oft hilfreiche Leitlinien oder sogar Tabellen, die als Vorlagen oder Checklisten für die Konformitätsbewertung dienen können.
Tipp 4: Ein Testplan braucht einen Entwurf, und der Prototyp braucht Vorversuche.
Die Essential Performance und die Risikoanalyse werden sich auf die Testanforderungen auswirken. Daher ist es wichtig, dass diese vor dem Testplan erstellt werden.
Wahrscheinlich gibt es viele Tests, die nicht anwendbar sind. Helbling-Experten empfehlen, sie als solche zu kennzeichnen und eine Begründung hinzuzufügen. So werden spätere Audits oder Überprüfungen vereinfacht. Was nicht dokumentiert ist, wird nicht berücksichtigt.
Zu Beginn des Entwicklungszyklus sollten ein Isolationsdiagramm erstellt und die Spannungspegel angegeben werden, gegen die das Gerät geprüft werden muss. Diese Diagramme lassen sich sehr leicht mit Experten überprüfen und sind eine grosse Hilfe bei der Festlegung des Prüfplans.
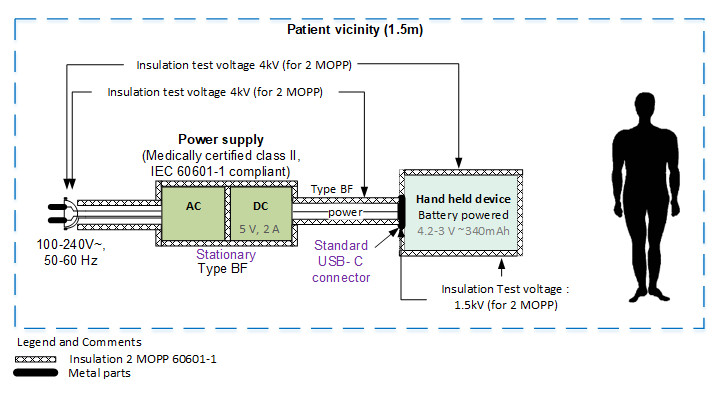
Die Norm verlangt die Durchführung der Zertifizierungstests mit einem repräsentativen Exemplar des Geräts. Dabei will sich niemand die Mühe machen, jedes Detail des Designs zu verfeinern, um dann wegen fehlgeschlagener Tests ein Re-Design durchführen zu müssen. Daher ist die Vorabprüfung bestimmter Aspekte im Zusammenhang mit der IEC 60601 in frühen Prototypen entscheidend.
Vorabtests in den eigenen Einrichtungen sind besonders hilfreich. In wenigen Stunden lässt sich abschätzen, inwieweit die Norm erfüllt wird und verschiedene Konstruktionslösungen können schnell bewertet werden.
Die Durchführung von Tests bei einer akkreditierten Prüfstelle ist dagegen in der Regel teuer und muss weit im Voraus geplant werden. Deshalb führt Helbling ESD-, EMV- und Ableitstromtests mit kalibrierten Geräten in eigenen Einrichtungen durch. Wenn es darum geht, ein Zertifikat zu erhalten oder tiefgreifende Kenntnisse über einen bestimmten Aspekt der Norm zu erlangen, arbeitet Helbling mit akkreditierten Prüfstellen zusammen, um die Tests durchzuführen.

Tipp 5: Die Dauer des Akkreditierungsverfahrens sollte im Projektplan berücksichtigt werden.
Die Dauer der verschiedenen Teile des Akkreditierungsverfahrens wird sehr oft unterschätzt. Ein häufiger Fehler besteht darin, die Gesamtdauer nur auf die Dauer der Prüfungen zu reduzieren.
Ein Grund: Prüfinstitute haben nur begrenzte kalibrierte Ressourcen wie etwa echolose Räume zur Verfügung. Die Verfügbarkeit des Testhauses sollte deshalb im Voraus gebucht werden, sonst entstehen Wartezeiten. Zudem müssen die kritischen Komponenten der medizinischen elektrischen Geräte wie Batterien oder Netzteile separat zertifiziert werden. In einigen Fällen ist kein Zertifikat vom Hersteller erhältlich und es müssen zusätzliche Prüfungen organisiert werden.
Generell ist die Zusammenstellung des Risikomanagement-Dossiers mit viel Arbeit verbunden. Wenn sie gemäss ISO 14971 erfolgte, ist der grösste Teil der Arbeit bereits erledigt. Diese Informationen müssen jedoch auch in das Prüfberichtsformular (CB-Schema-Dokument) übertragen oder in diesem abgebildet werden. Dadurch wird der Nachweis erbracht, dass die Risikomanagement-Datei die Anforderungen der geltenden Normenfamilie IEC 60601 erfüllt. Das Zusammentragen aller Informationen und das Ausfüllen dieses Prüfberichtsformulars kann leicht einen Monat oder mehr in Anspruch nehmen.
Abhängig von der definierten Anwendungsumgebung und dem Vorhandensein von Software kann die IEC 60601-Zertifizierung auch noch weitere Schritte notwendig machen: Zum Beispiel muss die Usability-Engineering-Datei in manchen Fällen gemäss IEC 62366 und die Softwareentwicklungsdatei gemäss IEC 62304 eingereicht werden. Diese Unterlagen sollten rechtzeitig bereitgehalten werden.
Letztlich kann die Prüfstelle nach der Analyse der Dokumentation noch Nichtkonformitätsberichte erstellen, die Anpassungen oder Ergänzungen in den Dossiers erfordern. Beispielsweise müssen Warnhinweise in der Gebrauchsanweisung und Sicherheitszeichen auf dem Produktetikett hinzugefügt werden.
Nach Abschluss der Tests und der Analyse der Unterlagen wird ein Bericht von der Prüfstelle ausgestellt, den ein unabhängiger Gutachter zur Prüfung erhält. Er bewertet, ob alles korrekt durchgeführt wurde, und gibt schliesslich das CB-Zertifikat für das Gerät frei. Dieser Vorgang hängt von der Verfügbarkeit der Experten ab, daher sollten ein bis vier Wochen für die Freigabe des CB-Zertifikats eingeplant werden.
Zusammenfassung: Frühe Integration der IEC60601-Normen in den Entwicklungsprozess ist ein Erfolgsfaktor
Die Berücksichtigung der IEC 60601-Normenfamilie zu einem frühen Zeitpunkt im Designprozess ist zwar eine Herausforderung, aber entscheidend für die Entwicklung sicherer medizinischer elektrischer Geräte. Helbling verfügt über umfassende Erfahrung in diesem Bereich: Mit moderner Infrastruktur und Ausrüstung beraten und unterstützen Expertenteams Unternehmen bei der Produktentwicklung, den Vortests und dem Zertifizierungsprozess.
Autoren: Laura Santos Carreras, Chantal Boyer Chardonnens, Stefan Bauer
Hauptbild: AdobeStock





